Adakveo vs Oxbryta: Să vă cunoașteți alternativele la crizanlizumab
Ultima actualizare: 15 ianuarie 2024
Puteți avea acces legal la medicamente noi, chiar dacă acestea nu sunt aprobate în țara dumneavoastră.
Aflați cum
În urma revocării autorizației Adakveo crizanlizumab) în UE, mulți pacienți și medici trebuie să găsească o alternativă la Adakveo .
Dacă ați răspuns bine la tratament, puteți accesa în continuare Adakveo chiar dacă nu mai este aprobat în UE. Cu toate acestea, dacă medicul dumneavoastră preferă să vă schimbe cursul tratamentului, este bine să înțelegeți ce înseamnă acest lucru pentru dumneavoastră ca pacient.
În acest articol ne vom uita la una dintre posibilele alternative la Adakveo pe care medicul dumneavoastră ar putea dori să o discute - Oxbryta voxelotor). Aici veți găsi o prezentare generală rapidă a asemănărilor și diferențelor dintre Adakveo și Oxbryta.
Adakveo vs Oxbryta: Pentru ce sunt utilizate?
Atât Adakveo , cât și Oxbryta sunt medicamente eliberate pe bază de prescripție medicală, indicate pentru tratamentul bolii falciforme 1,2. Cu toate acestea, fiecare dintre medicamente vizează un aspect diferit al bolii.
Adakveo vizează reducerea frecvenței crizelor vaso-ocluzive dureroase, în timp ce Oxbryta este utilizat pentru tratarea anemiei hemolitice la pacienții cu anemie falciformă 1,2.
Pentru ce vârstă este aprobat Oxbryta în UE?
Spre deosebire de Adakveo, care poate fi utilizat numai la pacienții cu vârsta de până la 16 ani, Oxbryta este indicat și pentru pacienții pediatrici.
În SUA, Oxbryta poate fi prescris de la vârsta de 4 ani, în timp ce în UE, utilizarea pediatrică este aprobată numai de la vârsta de 12 ani 1,2.
Crizanlizumab vs Voxelotor: Cum funcționează?
Deși ambele medicamente vizează reducerea complicațiilor bolii falciforme, ele vizează aspecte diferite ale bolii.
Adakveo și reducerea crizelor dureroase
Adakveo își propune să reducă frecvența crizelor dureroase, care apar atunci când celulele sanguine malformate rămân blocate în vasele de sânge.
Ingredientul activ al medicamentului, crizanlizumab, este un tip specific de proteină cunoscut sub numele de anticorp monoclonal. Această proteină este formulată pentru a se lega de P-selectină, o substanță care se găsește pe stratul exterior al celulelor care căptușesc vasele de sânge.
P-selectina ajută celulele să se lipească de vasele de sânge și este implicată în blocarea vaselor în timpul episoadelor dureroase din boala falciformă. Prin conectarea la P-selectină și inhibarea funcției acesteia, Adakveo își propune să prevină aceste episoade dureroase 3.
Oxbryta și prevenirea anemiei
Oxbryta, pe de altă parte, vizează prevenirea anemiei asociate cu boala celulelor falciforme.
Ingredientul activ din Oxbryta, voxelotor, sporește capacitatea hemoglobinei de a reține oxigenul și o împiedică să formeze lanțuri rigide în vasele de sânge. Acest lucru ajută celulele roșii din sânge să își păstreze forma și flexibilitatea normale. De asemenea, reduce rata de distrugere prematură a acestora și le prelungește durata de viață 4.
Cât de eficiente sunt Adakveo și Oxbryta?
Eficacitatea Adakveo crizanlizumab) și Oxbryta voxelotor) a fost studiată în studii clinice.
-
Rezultatele studiului clinic Adakveo
Aprobarea FDA pentru Adakveo, precum și autorizația sa inițială de comercializare în UE s-au bazat pe rezultatele studiului clinic SUSTAIN. Studiul a comparat Adakveo (cu sau fără hydoxyurea) cu placebo.
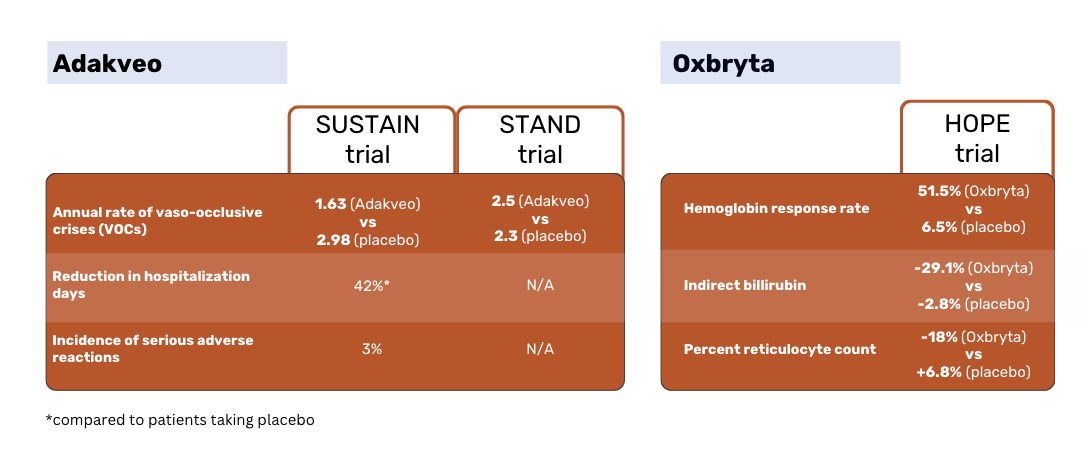
Conform rezultatelor studiului SUSTAIN, pacienții tratați cu Adakveo au avut o rată anuală mediană mai scăzută, semnificativă din punct de vedere statistic, a crizelor vaso-ocluzive (VOC) - 1,63 față de 2,98 pentru pacienții placebo. 36% dintre pacienții cu Adakveo din cadrul studiului nu au avut COV-uri pe parcursul perioadei de studiu de 52 de săptămâni, comparativ cu 17% dintre pacienții cu placebo 1.
Care au fost rezultatele procesului Adakveo STAND?
Studiul STAND global de fază 3, care a comparat din nou Adakveo cu placebo, nu a reușit să demonstreze o diferență semnificativă din punct de vedere statistic în ceea ce privește rata COV-urilor între grupurile de pacienți. Pacienții tratați cu Adakveo au avut în medie 2,5 crize dureroase în decurs de un an de tratament - fără a fi semnificativ diferit de cele 2,3 crize în medie raportate în grupul placebo 3.
Rezultatele neconvingătoare ale procesului STAND au stat la baza revocăriiAdakveo în UE.
-
Rezultatele studiului clinic Oxbryta
În studiul HOPE, Oxbryta a fost testat comparativ cu placebo. Eficacitatea s-a bazat pe ratele de răspuns ale hemoglobinei (Hb) definite ca o creștere a Hb de >1 g/dL de la momentul inițial până la Săptămâna 24.
Pacienții Oxbryta au avut o rată de răspuns de 51,1% față de 6,5% pentru pacienții placebo. Bilirubina indirectă a scăzut cu 29,1% la pacienții Oxbryta , comparativ cu o scădere cu 2,8% la pacienții placebo. Numărul procentual de reticulocite a scăzut cu 18% la pacienții Oxbryta și a crescut cu 6,8& la pacienții placebo 2.
După cum arată datele comune, nu este posibil să se facă o comparație directă între cele două medicamente, deoarece în studiile lor clinice au fost utilizate criterii de eficacitate diferite. Deoarece ambele tratamente abordează boala falciformă într-un mod diferit, este probabil ca Oxbryta să nu fie un înlocuitor direct al Adakveo, ci mai degrabă o parte a unui nou plan de tratament pe care medicul dumneavoastră îl va elabora pentru dumneavoastră.

Adakveo vs Oxbryta: Siguranță și efecte secundare
Conform informațiilor lor de prescriere, acestea sunt cele mai frecvente reacții adverse ale Adakveo și Oxbryta:
Efecte secundare ale Adakveo
- Greață
- Dureri articulare
- Dureri de spate
- Dureri de stomac
- Febra1.
În timpul studiului SUSTAIN, 3% dintre pacienți au prezentat reacții legate de perfuzie, caracterizate prin simptome precum dureri de cap, frisoane, vărsături, diaree, dificultăți de respirație sau wheezing 1.
Oxbryta efecte secundare
- Durere de cap
- diaree
- Dureri de stomac
- Greață
- Erupție cutanată
- Febra 2.
Mai puțin de 1% dintre pacienții din studiile clinice au prezentat reacții grave de hipersensibilitate, inclusiv erupții cutanate, dificultăți ușoare de respirație, umflături faciale ușoare și eozinofilie (creșterea numărului de globule albe)2.
Adakveo vs Oxbryta: Comparație de prețuri
În ceea ce privește prețurile medicamentelor care nu sunt încă aprobate sau disponibile, trebuie să le considerați doar orientative. Prețul final poate varia în funcție de locația dumneavoastră sau de furnizor.
Costuri Adakveo pe an
Doza recomandată pentru Adakveo este de 5 mg/kg de masă corporală la fiecare 4 săptămâni. Aceasta înseamnă 13 perfuzii pe an. Pentru o persoană care cântărește 60 kg, aceasta ar necesita 13 perfuzii x 300 mg de Adakveo sau 39 de fiole de medicament.
La un preț de aproximativ 5 214 EUR pe flacon de 100 mg, costul anual al unui tratament Adakveo se ridică la aproximativ 203 346 EUR 5.
Costurile Oxbryta pe an
Doza recomandată de Oxbryta pentru pacienții cu greutate corporală mai mare de 40 kg este de 1.500 mg de Oxbryta o dată pe zi, egală cu 3 comprimate x 500 mg fiecare.
Un pachet de 90 de comprimate de 500 mg costă aproximativ 40 365 EUR și este suficient pentru o lună, pe baza dozei recomandate mai sus. Prin urmare, costul anual al tratamentului cu Oxbryta se ridică la 484 380 EUR 6.
Unde sunt aprobate Adakveo și Oxbryta ?
Adakveo crizanlizumab) este aprobat în prezent în mai multe țări, inclusiv în SUA, Canada și Australia 7,9,10. Autorizația sa condiționată de introducere pe piață în UE a fost revocată în mai 2023 3.
Oxbryta voxelotor) este aprobat în SUA, UE și Canada 4,8,9. Cu toate acestea, în cadrul UE, Oxbryta nu este încă disponibil pe scară largă pe piață, deoarece timpul dintre autorizare și lansarea pe piață poate varia semnificativ în funcție de țară.
Adakveo sau Oxbryta nu sunt (mai) aprobate sau disponibile în țara dumneavoastră? Dacă dumneavoastră și medicul dumneavoastră sunteți de părere că aceste tratamente v-ar putea fi benefice, luați legătura cu echipa noastră de experți în accesul la medicamente. Vă putem oferi o ofertă de preț personalizată pentru procurarea medicamentului pentru dvs.
Referințe:
- PUNCTELE PRINCIPALE ALE INFORMAȚIILOR DE PRESCRIERE. Novartis, accesat la 27 septembrie 2023.
- PUNCTELE PRINCIPALE ALE INFORMAȚIILOR DE PRESCRIERE. Oxbryta, accesat la 27 septembrie 2023.
- Adakveo | Agenția Europeană pentru Medicamente. Agenția Europeană pentru Medicamente, accesat la 27 septembrie 2023.
- Oxbryta | Agenția Europeană pentru Medicamente. Agenția Europeană pentru Medicamente, accesat la 27 septembrie 2023.
- Cumpărați Adakveo (crizanlizumab) online. Everyone.org, accesat la 27 septembrie 2023.
- Cumpărați Oxbryta (voxelotor) online. Everyone.org, accesat la 27 septembrie 2023.
- Adakveo. Therapeutic Goods Administration (TGA), accesat la 27 septembrie 2023.
- FDA aprobă un medicament pentru tratarea bolii celulelor falciforme la pacienții pediatrici. FDA, 17 decembrie 2021.
- Medicamente noi aprobate în 2019 - Meds Entry Watch. Canada.ca, 10 februarie 2021.
- FDA aprobă prima terapie țintită pentru tratarea pacienților cu complicație dureroasă a bolii falciforme. FDA, 15 noiembrie 2019.