Poate Enhertu să trateze cancerul ovarian? Toate datele, dar nu toate balivernele.
Ultima actualizare: 15 iulie 2024
Puteți avea acces legal la medicamente noi, chiar dacă acestea nu sunt aprobate în țara dumneavoastră.
Aflați cumEnhertu (fam-trastuzumab deruxtecan-nxki) a fost aprobat pentru prima dată de FDA în 2019 1. La acel moment, a fost indicat pentru tratamentul cancerului de sân HER2-pozitiv. De atunci, Enhertu a fost aprobat pentru mai multe indicații. Acestea includ cancerul gastric HER2-pozitiv, cancerul mamar HER2-jos și cancerul pulmonar cu celule non-smici HER2-mutant. Din aprilie 2024, tratamentul este, de asemenea, aprobat de FDA pentru utilizare în toate tumorile HER2-pozitive5.
În acest context, Enhertu a atras o mare atenție din partea mass-media. Ca o consecință firească a acestei campanii, bolnavii de cancer de pretutindeni se întreabă dacă Enhertu poate fi aplicabil și în cazul lor.
Ca întotdeauna, suntem aici pentru a trece peste zgomot și a analiza datele disponibile. În acest articol, vom trece în revistă tot ce este de știut despre Enhertu pentru cancerul ovarian.
Ce tip de cancer tratează Enhertu ?
Pacienții de pretutindeni se întreabă dacă Enhertu poate vindeca toate tipurile de cancer. Din păcate, nu este cazul. Și nu este cazul în mod intenționat. Enhertu este o terapie țintită special pentru:
- Tumori cu expresie HER-2. HER-2 este o proteină care se găsește pe suprafața diferitelor tipuri de celule din organism. Aceasta ajută la creșterea normală a celulelor. Cu toate acestea, în anumite tipuri de cancer, poate deveni hiperactivă din cauza unor modificări genetice sau mutații. Supraexpresia HER2 afectează între 2% și 66% din cazurile de cancer ovarian 5.
- Tumori care s-au răspândit în alte părți ale corpului și/sau sunt inoperabile 4. Studiile clinice viitoare ar putea implica Enhertu în stadii mai timpurii ale tratamentului cancerului 6. Cu toate acestea, acest lucru nu este cazul în prezent.
Cât de eficient este Enhertu pentru cancerul ovarian?
Studiul DESTINY-PanTumor02, aflat în curs de desfășurare în faza 2, se concentrează pe testarea activității Enhertu în diferite tipuri de cancere solide HER2-pozitive. Unul dintre acestea este cancerul ovarian. Rezultatele intermediare ale studiului au fost împărtășite în iunie 2023 și se arată promițătoare.
Pentru pacientele cu cancer ovarian, rezultatele preliminare cheie ale studiului sunt:
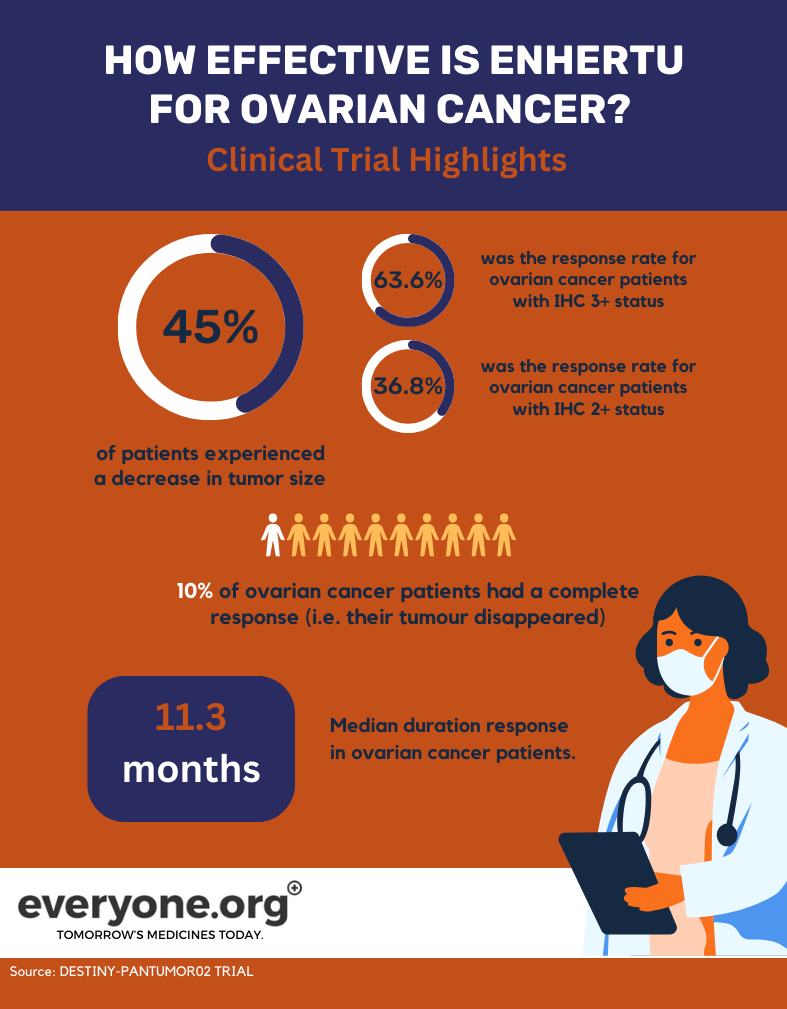
- Rata globală de răspuns a fost de 45,0%. Ceea ce înseamnă că la 45% dintre pacienții tratați cu Enhertu tumorile s-au micșorat. Pentru pacienții cu un statut HER2 IHC 3+, rata globală de răspuns a fost de 63,6%. Pentru cei cu statut IHC 2+, rata de răspuns a fost de 36,8% 3.
- 10% dintre pacientele cu cancer ovarian au avut un răspuns complet. Cu alte cuvinte, tumora lor a dispărut complet 3.
- După 12 luni, 45,8% dintre pacientele cu cancer ovarian cu tumori care au scăzut în dimensiune sau au dispărut au raportat că încă mai beneficiau de acest beneficiu3.
- Durata mediană a răspunsului la pacientele cu cancer ovarian a fost de 11,3 luni3.
În general, aceste rezultate pot fi considerate încurajatoare. Durata îndelungată a răspunsurilor este un rezultat deosebit de notabil, potrivit Dr. Meric-Bernstam (președinte al Departamentului de investigații terapeutice în domeniul cancerului de la MD Anderson Cancer Center din SUA) 3.
Pe baza rezultatelor acestor studii clinice, FDA din SUA a acordat Enhertu prima sa aprobare pentru un medicament care să fie utilizat în toate cancerele cu expresie HER2.

Când va fi aprobat Enhertu pentru cancerul ovarian?
Începând cu aprilie 2024, Enhertu este aprobat pentru toate cancerele care exprimă HER2, inclusiv cancerul ovarian.
Studiul DESTINY-PanTumor02 este în curs de desfășurare, rezultatele finale fiind așteptate în aprilie 2027 7. Cu toate acestea, rezultatele preliminare ale studiului au fost deja suficiente pentru recenta aprobare pan-tumorală a FDA.
Dacă vă aflați în afara SUA, statutul de aprobare al Enhertu pentru cancerul ovarian poate fi diferit.
Poate medicul meu să prescrie Enhertu pentru cancer ovarian?
Cel mai bun răspuns în prezent este "poate".
Începând cu iulie 2024, Enhertu a fost aprobat numai în SUA pentru tratamentul cancerului ovarian HER2-pozitiv. Cu toate acestea, chiar și în alte țări, medicul dumneavoastră are autoritatea de a prescrie oricum medicamentul pentru această indicație. Ar putea face acest lucru pe baza rezultatelor preliminare ale studiului clinic DESTINY-PanTumor02 și pe baza particularităților cazului dumneavoastră.
Atunci când un medic prescrie un medicament pentru tratarea unei boli pentru care acesta nu este (încă) aprobat la nivel local, aceasta se numește utilizare off-label. O rețetă pentru o utilizare off-label poate fi dificil de eliberat în unele țări, în funcție de reglementările locale și de disponibilitate. Cu toate acestea, este întotdeauna posibil să o eliberați utilizând regulamentul privind importul pacientului desemnat.
Medicul dumneavoastră a luat decizia de a vă prescrie Enhertu pentru tratamentul cancerului ovarian? Echipa noastră de la www.everyone.org vă poate ajuta să accesați acest medicament. Suntem specializați în procurarea și livrarea medicamentelor prescrise neaprobate sau indisponibile în țara pacientului. Contactați-ne, ca să vă putem ajuta.
Referinţe:
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Istoricul aprobării FDA. Drugs.com, 15 august 2022.
- Terapie revoluționară. FDA, 4 ianuarie 2018.
- Doherty, Kyle. Enhertu este promițător pentru cancerele solide greu de tratat. Cure Today, 6 iunie 2023.
- USPI-DB-04 CDX Update FINAL. Daiichi Sankyo, accesat la 3 octombrie 2023.
- Teplinsky, Eleonora și Franco Muggia. EGFR și HER2: există un rol în cancerul ovarian?, Translational Cancer Research, 13 februarie 2015.
- Liu, Angus. ASCO: Enhertu oferă o activitate pan-tumorală "foarte convingătoare". Fierce Pharma, 5 iunie 2023.
- A Phase 2 Study of T-DXd in Patients With Selected HER2 Expressing Tumors (DPT02), ClinicalTrials.gov, accesat la 03 octombrie 2023.