Enhertu pentru cancerul pulmonar: Unde este aprobat și cum să îl obțineți?
Ultima actualizare: 15 iulie 2024
Puteți avea acces legal la medicamente noi, chiar dacă acestea nu sunt aprobate în țara dumneavoastră.
Aflați cumEnhertu fam-trastuzumab deruxtecan-nxki) a fost unul dintre tratamentele pentru cancer de urmărit, încă de la prima sa aprobare de către FDA în 2019 1.
Deoarece siguranța și eficacitatea Enhertu în cancerul ovarian și cancerul colorectal sunt încă în curs de investigare, medicamentul este deja aprobat pentru mai multe indicații. Inclusiv cancerul mamar HER2-pozitiv, cancerul gastric HER2-pozitiv și cancerul mamar HER2-jos. FDA a aprobat, de asemenea, Enhertu pentru cancerul pulmonar cu celule non-small HER2-mutant. CHMP din Europa a dat recent un aviz pozitiv pentru a face același lucru în cadrul UE 2.
Dacă sunteți pacient cu cancer pulmonar în Regatul Unit sau în altă parte în afara SUA și a UE, probabil vă întrebați când va fi disponibil Enhertu și pentru dvs.
Iată tot ce trebuie să știți despre Enhertu pentru cancerul pulmonar și la ce se pot aștepta pacienții din Regatul Unit și din restul lumii.
Care este indicația pentru Enhertu pentru cancerul pulmonar?
Ca terapie țintită, Enhertu este destinat numai tratării cancerelor cu o mutație HER2. Ca atare, tratamentul se aplică la aproximativ 2% din toți pacienții cu NSCLC 3.
Enhertu este indicat ca monoterapie la pacienții adulți cu NSCLC avansat ale căror tumori au o mutație HER2 (ERBB2) activatoare. Enhertu se adresează pacienților care au primit anterior o terapie sistemică și al căror cancer fie s-a răspândit în alte părți ale corpului, fie nu poate fi îndepărtat chirurgical 2.
Care este rata de succes a Enhertu pentru cancerul pulmonar?
Studiul de fază II DESTINY-Lung02 în curs de desfășurare investighează siguranța și eficiența Enhertu în tratarea NSCLC cu mutație HER2. În cadrul studiului, sunt comparate două doze de Enhertu (5,4 mg/kg și 6,4 mg/kg).
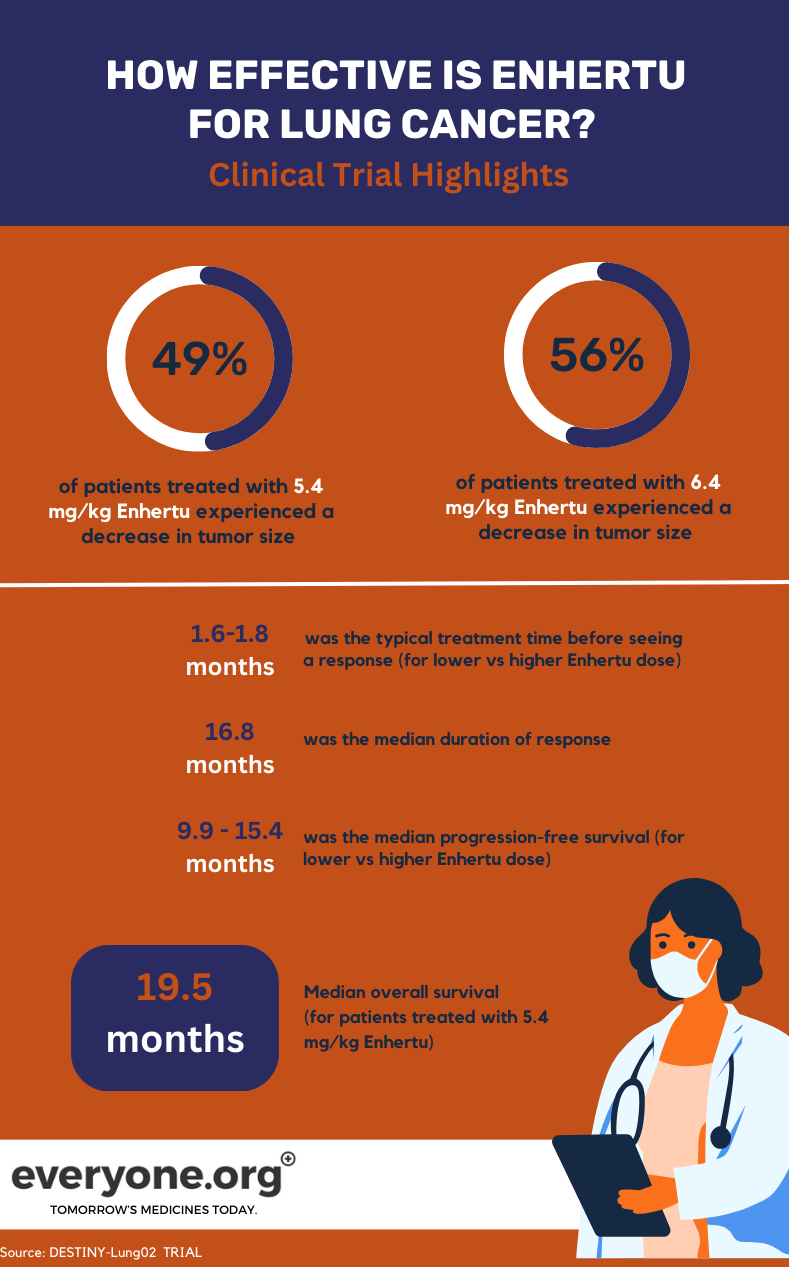
Pentru pacienții cu cancer pulmonar, principalele rezultate preliminare ale studiului DESTINY-Lung02 sunt:
- Tumorile s-au micșorat la 49% dintre pacienții tratați cu doza mai mică de Enhertu și la 56% dintre cei tratați cu doza mai mare.
- Tumorile au dispărut complet la 1% și 4% dintre pacienții din grupul cu doze mai mici și, respectiv, mai mari.
- Durata mediană a răspunsului a fost de 16,8 luni pentru pacienții din grupul cu doza mai mică Enhertu . Pentru pacienții din celălalt grup, DoR a fost raportată ca neestimabilă.
- Timpul median necesar pentru observarea răspunsului inițial la tratament a fost de 1,8 luni și 1,6 luni în grupul cu doze mai mici și, respectiv, mai mari.
- Supraviețuirea mediană fără progresie a fost de 9,9 luni la 5,4 mg/kg și de 15,4 luni la 6,4 mg/kg 4.
Care a fost supraviețuirea mediană pentru pacienții Enhertu ?
Pentru pacienții care au primit doza mai mică de Enhertu în studiul clinic, supraviețuirea globală mediană (SG) a fost de 19,5 luni. OS a fost raportată ca neputând fi estimată pentru grupul cu doza mai mare 4.
Care sunt efectele secundare ale Enhertu asupra plămânilor?
La pacienții cu Enhertu au fost raportate unele cazuri severe, cu risc vital sau fatale de boală pulmonară interstițială (ILD). Pacienții cu insuficiență renală moderată pot prezenta un risc mai mare 6.
În cadrul studiului DESTINY-Lung02, ILD a fost raportată la 12,9% dintre pacienții din grupul cu doza mai mică și la 28% dintre pacienții din grupul cu doza mai mare. Majoritatea acestor cazuri nu au fost severe. ILD de gradul 3 sau mai mare a fost raportată la 2% dintre pacienții din ambele grupuri de pacienți.
Profilul de siguranță al Enhertu pentru cancerul pulmonar este similar cu performanța sa în alte indicații. Pe baza incidenței mai scăzute a efectelor adverse (38,6% vs 58%), doza de 5,4 mg/kg este considerată tratamentul optim pentru pacienții cu NSCLC 4.

Unde este aprobat Enhertu pentru cancerul pulmonar?
În prezent, Enhertu este aprobat în SUA, UE, Israel și Japonia pentru tratamentul pacienților adulți cu NSCLC nerezecabil sau metastatic ale căror tumori prezintă mutații HER2 (ERBB2) activatoare 4.
Este Enhertu aprobat pentru cancerul pulmonar în Marea Britanie?
Începând din iulie 2024, nu încă. Un proiect final de orientare publicat de NICE în martie 2024 a anunțat că Enhertu nu va fi pe NHS până când nu este disponibil un preț rentabil. Între timp, din păcate, Enhertu nu este disponibil în Marea Britanie pentru cancerul pulmonar 7.
Medicul meu poate prescrie Enhertu pentru cancerul pulmonar dacă nu este încă aprobat?
Răspunsul scurt este da.
Enhertu a fost deja aprobat în mai multe țări pentru tratamentul NSCLC cu mutație HER2. Pe baza acestui fapt, medicul dumneavoastră are autoritatea de a prescrie medicamentul pentru această indicație, chiar dacă acesta nu este încă aprobat în țara dumneavoastră.
Atunci când un medic prescrie un medicament pentru tratarea unei boli pentru care acesta nu este aprobat (încă), aceasta se numește utilizare off-label. O rețetă pentru utilizare în afara etichetei poate fi dificil de eliberat în unele țări, în funcție de reglementările locale și de disponibilitate. Cu toate acestea, este întotdeauna posibil să o eliberați utilizând regulamentul privind importul pacientului desemnat.
Medicul dumneavoastră a luat decizia de a vă prescrie Enhertu pentru tratamentul cancerului pulmonar? Echipa noastră de laeveryone.org vă poate ajuta să aveți acces la medicament. Suntem specializați în procurarea și livrarea de medicamente prescrise neaprobate sau indisponibile în țara pacientului. Contactați-ne, astfel încât să vă putem ajuta.
Referințe:
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Istoricul aprobării FDA. Drugs.com, 15 august 2022.
- Enhertu. Agenția Europeană pentru Medicamente, accesat la 06 noiembrie 2023.
- HER2 și cancerul pulmonar. American Lung Association, accesat la 6 noiembrie 2023.
- Enhertu a demonstrat răspunsuri tumorale puternice și durabile în cancerul pulmonar avansat HER2-mutant tratat anterior în studiul de fază II DESTINY-Lung02. AstraZeneca, 11 septembrie 2023.
- Informații despre proiect | Trastuzumab deruxtecan pentru tratamentul cancerului pulmonar cu celule non-scuamoase cu mutație HER2 nerezecabil sau metastatic după una sau mai multe terapii [ID3934] | Ghid. NICE, accesat la 6 noiembrie 2023.
- USPI-DB-04 CDX Update FINAL. Daiichi Sankyo, accesat la 6 noiembrie 2023.
- UK NICE rejects Daiichi Sankyo's Enhertu for breast cancer, Pharmaceutical Technology, accesat la 15 iulie 2024.